
A continuación, se analizan los trabajos más destacados presentados en el Congreso Virtual 2020 de la Sociedad Europea de Oncología Médica (ESMO), celebrado del 19 al 21 de septiembre, con resultados interesantes y propuestas innovadoras para continuar generando conocimiento útil en favor de los pacientes con sarcoma.
Estudio AcSé
Jean-Yves Blay (Lyon, Francia).
Pembrolizumab demostró beneficio clínico como agente único en el tratamiento de pacientes con subtipos histológicos raros de sarcoma. (1)
El estudio AcSé es un ensayo clínico fase II, no aleatorizado, abierto, multicéntrico, cuyo objetivo es evaluar la eficacia y seguridad del tratamiento con pembrolizumab como agente único. Los subtipos evaluados fueron sarcomas raros, con una incidencia menor a 0.2 casos por 100 000 individuos al año. Los pacientes elegibles fueron mayores de 18 años, con buen estado funcional (ECOG ≤1) y enfermedad avanzada resistente al tratamiento estándar. Participaron 80 pacientes agrupados según el subtipo histológico, incluyendo cordoma (n= 24), sarcoma alveolar de tejidos blandos (n= 13), tumor desmoplásico de células redondas pequeñas (n= 6), tumor similar a rabdoide maligno con inactivación de SMARCA4 (n= 6) y otros histotipos (n= 31). (1)
Los pacientes recibieron pembrolizumab a dosis de 200 mg por infusión intravenosa durante 30 minutos, cada 21 días, durante un máximo de 2 años. El criterio de valoración principal del estudio fue la tasa de respuesta objetiva con base en RECIST 1.1. Los criterios de valoración secundarios incluyeron la tasa de beneficio clínico, duración de la respuesta, supervivencia libre de progresión (SLP), supervivencia global, (SG) y la seguridad. (1)
Con una mediana de 5 ciclos (rango de 1 a 33), desde julio de 2017 hasta febrero de 2020, el análisis de eficacia mostró que el mejor resultado fue la respuesta parcial observada en 13 pacientes (16.25%) y enfermedad estable en 29 pacientes (36.25%). Fue relevante observar que la respuesta dependió del subtipo histológico, siendo el grupo de pacientes con tumor similar a rabdoide maligno con inactivación de SMARCA4 el que tuvo mayor número de respuestas (50%), seguido por el sarcoma alveolar (39%) con una diferencia estadísticamente significativa con respecto a los demás grupos. (1)
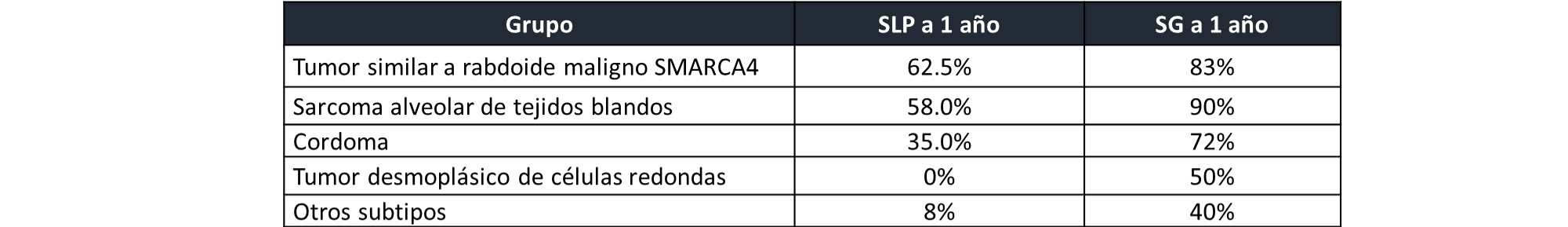
La respuesta mencionada se reflejó en las tasas de supervivencia con una diferencia significativa (p= 0.00016) donde la mediana de SLP no se alcanzó (62.5% a un año, hasta el punto de corte de los datos) para el tumor similar a rabdoide maligno con inactivación de SMARCA4, seguido por el sarcoma alveolar (14 meses), el cordoma (5.7 meses), el tumor desmoplásico de células redondas pequeñas (5 meses) y otros subtipos histológicos (2.7 meses). (1)
La mediana de SG se alcanzó en 3 de los 5 grupos, con una mediana de 20 meses en la cohorte de cordoma, 7.4 meses en el tumor desmoplásico de células redondas pequeñas y de 5.4 meses en el grupo de otros histotipos. (1)
Con respecto al criterio de valoración de seguridad, se informó la suspensión del ensayo después de recibir una mediana de 4 ciclos en 54 pacientes (67.5%). La muerte acaeció en 28 pacientes después de recibir una mediana de 3 ciclos. (1)
Pembrolizumab mostró beneficio clínico y actividad prolongada en subtipos seleccionados de sarcomas raros. Estas respuestas en sarcomas no se asociaron de manera consistente con la expresión de PD-L1, carga mutacional tumoral alta o infiltrados celulares, requiriendo mayor investigación traslacional. (1)
Estudio REGOBONE
Florence Duffaud (Marsella, Francia).
El estudio REGOBONE es un ensayo clínico fase II, aleatorizado, doble ciego, no comparativo, controlado con placebo, que evalúa la seguridad y eficacia de regorafenib en 5 cohortes paralelas, independientes, de sarcomas óseos. Durante el Congreso de ESMO se presentaron los resultados de la cohorte de pacientes con sarcoma de Ewing metastásico recurrente, con el antecedente de haber obtenido buenos resultados en las cohortes de osteosarcoma y condrosarcoma. (2)
Se incluyó a pacientes con edad igual o mayor a 10 años, con 1 a 2 líneas previas de quimioterapia para enfermedad metastásica y buen estado funcional con ECOG 0-1. Los pacientes elegibles fueron aleatorizados 2:1, asignando regorafenib, en el brazo experimental, a dosis de 160 mg/día durante 3 semanas y suspendiendo una semana y placebo, en el brazo control, emparejado con cruzamiento opcional en el momento de confirmar la progresión de la enfermedad. (2)
El objetivo primario fue comparar la tasa libre de progresión a las 8 semanas, evaluado de manera central con base en RECIST 1.1. Los criterios de valoración secundarios fueron la SLP, SG y la seguridad. (2)
Desde septiembre de 2014 hasta noviembre de 2019 se incluyeron 41 pacientes, teniendo 36 evaluables para eficacia: 13 en el brazo con placebo y 23 en el brazo con regorafenib. (2)
En cuanto al objetivo primario, 13/23 pacientes (56.5%) en el grupo de regorafenib no progresaron a las 8 semanas, en comparación con 1/13 pacientes (7.7%) en el grupo con placebo. La mediana de SLP fue de 11.4 (IC 95% de 4.6 a 22.9) vs. 3.9 (IC 95% de 3.3 a 7.3) semanas para los brazos de regorafenib y placebo, respectivamente. En 5 pacientes (21.7%) se alcanzó respuesta parcial con regorafenib. La mediana de SG fue de 34.9 semanas para regorafenib vs. 30.4 semanas para placebo.
Los eventos adversos grado ≥3 más frecuentes relacionados con regorafenib, durante el período doble ciego, fueron diarrea (13%), toxicidad cutánea (13%), astenia (9%), trombocitopenia (9%), mucositis (9%) y neutropenia febril (9%). Solo hubo una muerte (4.5 %) asociada con trombocitopenia. (2)
Regorafenib demostró actividad para retrasar la progresión de la enfermedad en pacientes con sarcoma de Ewing metastásico tras la falla con la quimioterapia convencional. A pesar de una tasa libre de progresión menor a las 8 semanas esperadas, este estudio aleatorizado mostró una señal prometedora del beneficio de regorafenib ante la recaída y con un perfil de toxicidad moderado. (2)
Estudio TRAMUNE
Maud Toulmonde (Burdeos, Francia).
Trabectedina en combinación con durvalumab demostró actividad antineoplásica en el tratamiento de pacientes con sarcoma de tejidos blandos irresecable o metastásico. (3)
El estudio TRAMUNE es un ensayo clínico fase Ib, multicéntrico, que evalua la seguridad y eficacia preliminar (en términos de respuesta objetiva) de la combinación de trabectedina y durvalumab en el tratamiento de pacientes con sarcoma de tejidos blandos irresecable o metastásico pretratados con al menos una línea de quimioterapia (incluyendo antraciclinas y pacientes con cáncer de ovario recurrente).
El diseño del estudio incluyó una fase inicial con escalamiento de dosis para trabectedina bajo un modelo convencional 3+3 y la integración de dos cohortes de expansión dentro de un diseño de Gehan en dos etapas. (3)
El objetivo principal fue evaluar la seguridad, las toxicidades limitantes de la dosis, la dosis máxima tolerada y la dosis recomendada para desarrollar un ensayo fase II. Los objetivos secundarios comprendieron la actividad antitumoral de la combinación en términos de tasa de respuesta objetiva, tasa libre de progresión a 6 meses, SLP con base en RECIST 1.1 y SG, explorando los biomarcadores inmunes en biopsias tumorales seriadas y metabolómica en muestras de plasma. (3)
La combinación se administró cada tres semanas de la siguiente forma: trabectedina en el día 1 del ciclo mediante perfusión por 3 horas, y durvalumab a dosis fija de 1,120 mg, administrado el día 2 del ciclo. Se incluyeron 40 pacientes mayores de 18 años, 9 de ellos en la fase de escalamiento de dosis (3 a 1.0 mg/m2 y 6 a 1.2 mg/m2), 15 en la cohorte de cáncer ovárico y 16 en la cohorte de sarcoma de tejidos blandos. (3)
En la fase inicial de escalamiento, la dosis máxima tolerada para trabectedina en combinación con durvalumab fue de 1.2 mg/m2, teniendo como toxicidad limitante de dosis el incremento de alanina aminotransferasa en grado 4, la cual resolvió a grado 1 en 9 días. En la cohorte de expansión de sarcoma de tejidos blandos (n= 16), la mediana de seguimiento fue de 10.7 meses. Se evaluó la seguridad en los 16 pacientes y la eficacia en 14. (3)
Los eventos adversos más frecuentes fueron náusea grado 1-2 (15.1%) y fatiga grado 1-2 (11.3%). Ocho pacientes (50%) tuvieron eventos adversos de grado 3-4, con frecuente disminución del recuento de neutrófilos (35.7%) y se reportaron dos eventos grado 5 con fallo multiorgánico y aplasia febril. (3)
En lo referente a la actividad antitumoral, seis pacientes (42.9 %) experimentaron una reducción del tamaño tumoral, documentando un caso de RP(leiomiosarcoma). Hubo cuatro casos con enfermedad estable (57%), una tasa de respuesta objetiva del 7.1% y una tasa libre de progresión a los 6 meses de 28.6%. (3)
Finalmente, la expresión de PD-L1 y la expresión de CD8 fueron bajas. La densidad basal de células CD163+ no se correlacionó con la reducción del tumor. Se describió una tendencia para la relación CD8 alto / CD163 bajo, como un posible perfil tumoral asociado con una mayor SLP, observación que requiere mayor fundamento científico. (3)
La combinación de trabectedina y durvalumab tiene actividad antitumoral en el tratamiento de los pacientes con sarcoma de tejidos blandos. La dosis máxima tolerada para trabectedina en combinación con durvalumab fue de 1.2 mg/m2. El perfil de seguridad mostró toxicidad gastrointestinal, citólisis hepática y neutropenia como los principales eventos adversos. (3)
Referencias:
Dr. Jorge Adán Alegría Baños – Dr. Jorge Luis Martínez Tlahuel
Oncólogos Médicos
Instituto Nacional de Cancerología
Ciudad de México, México
¿No tienes una cuenta? Regístrate