
En México el cáncer de mama ocupa el primer lugar por número de pacientes diagnosticados, con 29,929 casos en el 2020 y 7,931 muertes registradas [1]. En países desarrollados el diagnóstico se realiza principalmente en etapas tempranas; sin embargo, en México la realidad es otra, ya que se diagnostican pacientes principalmente en etapas avanzadas, donde el 50% corresponden a etapas localmente avanzadas y el 13.5% a etapas metastásicas [2]. Debido a que se diagnostican en etapas avanzadas, la tasa de supervivencia en el país es menor (datos a 5 años del 25% en etapas metastásicas [3]). No obstante, este panorama adverso ha cambiado con el advenimiento de nuevos fármacos, en específico para las pacientes que tienen diagnóstico de cáncer de mama con expresión de receptores hormonales positivos, que son aproximadamente el 70%.
Anteriormente, la expectativa de control de la enfermedad con fulvestrant como monoterapia era de 16 meses aproximadamente [4]. Actualmente, con la incorporación de los inhibidores de cinasas dependientes de ciclinas CDK4/CDK6, como ribociclib, se está cambiando el paradigma del tratamiento en cáncer de mama metastásico [5] con receptores hormonales positivos, debido a que ha logrado aumentar significativamente el tiempo a la progresión a 27 meses [6], además de haber demostrado beneficio en supervivencia global [7].
Los inhibidores de cinasa CDK4/6 actúan sobre la vía de proliferación celular CDK4/6-Cyc D1-pRB. Se ha observado que el cáncer con receptores de estrógenos positivos tiene altos niveles de la ciclina D1 (Cyc D1) [8], debido a la amplificación del gen CCND1. La sobreexpresión de Cyc D1 conlleva a la hiperactivación de la cascada de señalización del eje ciclina D1-cinasas dependiente de ciclina 4/6 (D-CDK4/6). El complejo Cyc D1-CDK4 fosforila a la proteína del retinoblastoma (pRb), se disocia del factor de transcripción E2F y, con ello, se activa a la ciclina E para unirse a la CDK2. Como consecuencia, se promueve la transición de la fase G1 a S del ciclo y conduce a la proliferación celular [8]. Ribociclib es un inhibidor de las cinasas CDK4/6 que induce un arresto en la fase G1 del ciclo celular y evita la fosforilación de la Cyc D1, lo que inhibe el crecimiento tumoral. Por tanto, la incorporación de ribociclib en combinación con letrozol, como se ha mencionado, aumenta el periodo libre de enfermedad y la supervivencia global en pacientes con cáncer de mama avanzado [8,9].
Diseño del estudio
Es un estudio clínico fase III, aleatorizado, doble ciego, comparado contra placebo (Figura 1), donde se incluyeron pacientes postmenopáusicas con cáncer de mama metastásico o irresecable con receptores hormonales positivos que no habían recibido tratamiento previo para enfermedad avanzada [10]. Se aleatorizaron 1:1 a 668 pacientes en dos grupos, donde se comparó el uso de 600 mg de ribociclib una vez al día durante 21 días consecutivos, en ciclos de 28 días, más 2.5 mg de letrozol una vez al día continuo (en el brazo experimental), vs. 3 tabletas al día de placebo por 21 días más 2.5 mg de letrozol al día continuo (brazo de control). Las pacientes recibieron el tratamiento hasta la progresión o la toxicidad inaceptable, muerte o interrupción por cualquier otro motivo. No se permitió el entrecruzamiento de brazos. Se permitió la reducción de dosis de ribociclib de 600 mg a 400 mg y a 200 mg.

Los criterios de inclusión fueron: mujeres postmenopáusicas con cáncer de mama recurrente o metastásico receptores hormonales positivos (RH+), HER2 negativo (HER2-), que no habían recibido terapia sistémica para la enfermedad avanzada. Las pacientes debían tener enfermedad medible según los criterios RECIST (Response Evaluation Criteria in Solid Tumors) o como mínimo una lesión que fuera predominantemente lítica, además de estado funcional ECOG (Eastern Cooperative Oncology Group) de 0 o 1 y función orgánica normal (hematológica, renal y hepática).
El objetivo principal del estudio era evaluar la supervivencia libre de progresión (SLP) según la versión 1.1 de RECIST, mientras que los objetivos secundarios fueron la supervivencia global (SG), la tasa de respuesta global (TRG, tasa de respuesta completa o parcial), la tasa de beneficio clínico (TRG más enfermedad estable durante al menos 24 semanas o más) y la seguridad [10].
Resultados
Se incluyeron 668 pacientes, de las cuales 334 recibieron ribociclib más letrozol y 334 recibieron placebo más letrozol. El 34% de las pacientes debutaron con enfermedad metastásica, mientras que el 65.9% presentó recurrencia de la enfermedad. Además, el 59% tenía enfermedad visceral y el 21% enfermedad ósea exclusiva. En el brazo experimental, el 76.9% de las pacientes interrumpieron ribociclib y el 39.5% letrozol, mientras que en el brazo de control el 40.6% de las pacientes interrumpieron el placebo y el 32.4% letrozol. Los principales motivos de interrupción del tratamiento fueron la progresión de la enfermedad (26% para ribociclib + letrozol vs. 44.7% para placebo + letrozol), decisión del paciente o investigador (6.6% vs. 7.8%) y eventos adversos (7.5% vs. 2.1%) [11].
El 50.6% de las pacientes del brazo de ribociclib redujeron la dosis debido a los eventos adversos (EA), con la neutropenia como EA más frecuente [11]. En general, el perfil de seguridad fue aceptable para la combinación de ribociclib + letrozol. Las principales toxicidades de grado III/IV fueron: neutropenia (59.3% ribociclib vs. 0.9% placebo), leucopenia (21% vs. 0.6%), hipertensión (9.9% vs. 10.9%), elevación de los niveles de alanina aminotransferasa (9.3% vs. 1.2%), linfopenia (6.9% vs. 0.9%) y elevación de los niveles de aspartato aminotransferasa (5.7% vs. 1.2%).
En el primer análisis interino, el ensayo alcanzó el principal criterio de valoración de SLP. Hubo una reducción estimada del 43.2% en el riesgo de progresión o muerte en el grupo de ribociclib + letrozol. Con una mediana de seguimiento de 26.4 meses, ribociclib más letrozol como terapia inicial demostró una mejora estadísticamente significativa en la SLP en pacientes (enero de 2017) [10,11].
La actualización final en ESMO 2021, mostró que la adición de ribociclib en primera línea en combinación con letrozol (Figura 2) prolongó la mediana de SG en más de 12 meses (63.9 meses para la combinación vs. 51.4 meses para letrozol solo [HR: 0.76; IC del 95%: 0.63-0.93; P= 0.004]). La duración media del seguimiento fue de 80 meses (punto de corte: junio de 2021), en donde el 92.4% de los pacientes habían interrumpido el tratamiento, de los cuales el 69.9% fue por la progresión de la enfermedad. Al corte, 9.0% de los pacientes del grupo de ribociclib seguían en tratamiento vs. 5.1% del grupo con placebo [7].
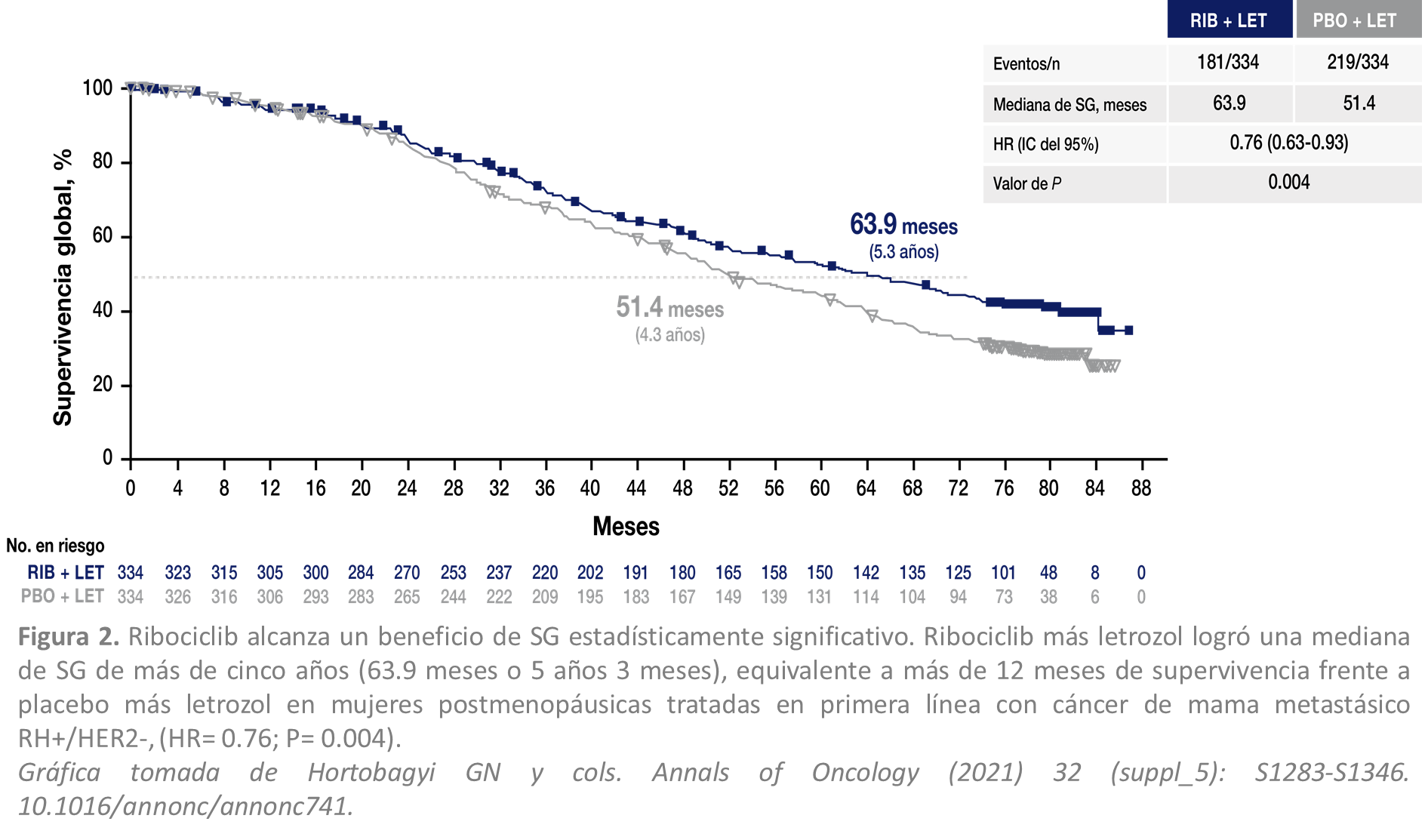
La tasa de SG de la combinación vs. solo letrozol a 4 años fue del 60.9% vs. 55.2%; a 5 años fue del 52.3% vs. 43.9% y a 6 años fue del 44.2% vs. 32.0%, respectivamente. El beneficio clínico neto aumenta conforme al tiempo y el beneficio es prolongado. El perfil de seguridad no cambió con la continuación del tratamiento a lo ya reportado previamente, por lo cual la mayoría de los eventos adversos ocurrieron en el primer año de tratamiento [7].
Conclusiones
El estudio mostró que dar ribociclib más letrozol prolonga la SG en más de 12 meses, en comparación con la monoterapia con letrozol. Aunque este resultado fue un objetivo secundario, nunca se habían reportado resultados tan promisorios como el que se demostró con el uso de ribociclib, sin importar la edad, si se utiliza el tratamiento en primera o segunda línea, o si se combina con un inhibidor de aromatasa o con fulvestrant, sigue conservando el beneficio de aumento de la SG. Pocos fármacos para el tratamiento de cáncer logran tener este tipo de resultados y, sobre todo, el beneficio en todos los subgrupos, con una excelente tolerabilidad y sin deterioro de la calidad de vida. Por lo tanto, ribociclib vino a cambiar la historia natural del cáncer de mama metastásico con RH+/HER2-, ya que ahora es una enfermedad crónica con supervivencias de más de cinco años, cambiando la vida de las pacientes y ofreciendo un aumento en la esperanza de vida.
Referencias:
Dr. Enrique Isay Talamantes Gómez
Oncólogo Médico
Ciudad de México, México
Gracias al apoyo educativo de Novartis México.
¿No tienes una cuenta? Regístrate